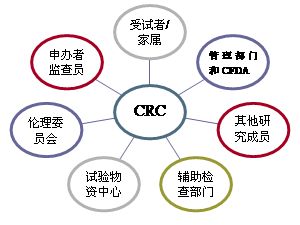
CRC團隊在研究中心協(xié)助臨床試驗機構(gòu)進行現(xiàn)場管理和具體操作的專業(yè)服務(wù),即臨床試驗現(xiàn)場管理組織(Site Management Organization, SMO)��,致力于通過提供臨床試驗相關(guān)的專業(yè)服務(wù)�,協(xié)助研究者和研究機構(gòu)承擔在臨床試驗中非醫(yī)生判斷類的事務(wù)性工作�����,提高臨床試驗質(zhì)量和進度,推動臨床試驗規(guī)范化進程����。
一�����、證標客CRC服務(wù)簡介
CRC團隊在研究中心協(xié)助臨床試驗機構(gòu)進行現(xiàn)場管理和具體操作的專業(yè)服務(wù)機構(gòu)��,即臨床試驗現(xiàn)場管理組織(Site Management Organization, SMO)�����,致力于通過提供臨床試驗相關(guān)的專業(yè)服務(wù)����,協(xié)助研究者和研究機構(gòu)承擔在臨床試驗中非醫(yī)生判斷類的事務(wù)性工作���,提高臨床試驗質(zhì)量和進度����,推動臨床試驗規(guī)范化進程���。
證標客的CRC團隊已經(jīng)在中國多個重要城市設(shè)有臨床研究協(xié)調(diào)員(Clinical Research Coordinator, CRC)服務(wù)網(wǎng)點�����,截止到2018年6月����,已經(jīng)擁有30多人的專業(yè)化團隊��,建立了國際標準的操作規(guī)程(SOPs)。團隊人員以護理��、醫(yī)學(xué)����、藥學(xué)等專業(yè)背景為主�����,熟悉ICH-GCP和GCP�����,經(jīng)過良好的SOP和其他技能培訓(xùn)����,英語水平良好,熟悉Inform, Datatrack, Medidata Rave等電子數(shù)據(jù)采集系統(tǒng)。
二、服務(wù)范圍
2.1 為申辦方/CRO提供的服務(wù)
? 項目可行性調(diào)研
? 倫理遞交
? 研究者會議組織
? 受試者招募
? 研究中心信息收集
? 試驗預(yù)算管理
? 研究相關(guān)培訓(xùn)
? 內(nèi)部稽查
? 臨床試驗項目管理
? 試驗物資和試驗文件管理
2.2 為研究機構(gòu)/研究者提供的服務(wù)
臨床試驗管理
? 專業(yè)臨床研究協(xié)調(diào)員(CRC)配備
? 研究文檔的管理
? 受試者招募與管理
? 研究物資管理
? 數(shù)據(jù)管理
? 倫理和機構(gòu)的溝通
? 安全信息的管理
研究中心管理
? 研究中心SOP的建立和完善
? 機構(gòu)認證輔導(dǎo)
? 研究者及其他參與人員的培訓(xùn)
? 協(xié)助機構(gòu)對在研項目的稽查
? 協(xié)助接受SFDA現(xiàn)場核查
? 費用協(xié)商