按照歐盟醫(yī)療器械分類規(guī)則����,IIa類醫(yī)療器械包含了眾多產(chǎn)品�,也是國內(nèi)出口型客戶問道的最多的產(chǎn)品類別之一�����。因此�����,本文為您介紹IIa類醫(yī)療器械CE認(rèn)證流程���。
引言:按照歐盟醫(yī)療器械分類規(guī)則���,IIa類醫(yī)療器械包含了眾多產(chǎn)品,也是國內(nèi)出口型客戶問道的最多的產(chǎn)品類別之一��。因此��,本文為您介紹IIa類醫(yī)療器械CE認(rèn)證流程�����。
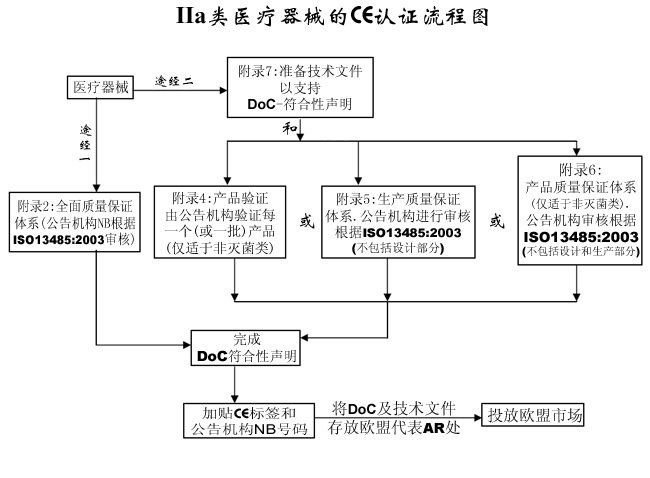
一����、IIa類醫(yī)療器械CE認(rèn)證流程:
1�、分類:確認(rèn)產(chǎn)品屬于IIa類醫(yī)療器械���;
2���、選擇符合性評估途徑:請參考下面的流程圖;
3�����、編制技術(shù)文件�����;
4���、委任歐盟授權(quán)代表�����;
5��、從第三方公告機(jī)構(gòu)(NB)獲得CE證書;
6、完成CE符合性聲明���;
7�、將技術(shù)文件存放在歐盟授權(quán)代表處(供歐盟主管機(jī)關(guān)隨時檢查)�;
8、建立(售后)警戒系統(tǒng) /加貼CE標(biāo)簽并將產(chǎn)品投放EEA市場�����。
二���、IIa類醫(yī)療器械CE認(rèn)證流程圖:
IIa類醫(yī)療器械CE認(rèn)證流程示意圖如下: