醫(yī)療器械唯一標識(UDI)的推廣應用����,是全球主要經(jīng)濟體醫(yī)療器械監(jiān)管大事件之一��,是醫(yī)療器械全生命周期管理的主線之一����。新醫(yī)療器械CE認證法規(guī)(MDR)的修訂要點��,自然也少不了UDI的要求����。
引言:醫(yī)療器械唯一標識(UDI)的推廣應用,是全球主要經(jīng)濟體醫(yī)療器械監(jiān)管大事件之一���,是醫(yī)療器械全生命周期管理的主線之一����。新醫(yī)療器械CE認證法規(guī)(MDR)的修訂要點�����,自然也少不了UDI的要求����。

一、什么是UDI����?
Unique device identifiers (UDIs) 器械唯一標識
-UDI 系統(tǒng)是醫(yī)療器械數(shù)據(jù)庫的一部分,目的是對醫(yī)療器械的識別提供一個全球協(xié)調(diào)化的框架�。
-UDI 是基于國際認可的器械標識和編碼標準創(chuàng)建的一系列數(shù)字或字母數(shù)字, 以便明確識別市場上的特定器械。
-UDI 由 UDI-DI 和 UDI-PI 組成�,必須標記在產(chǎn)品標簽、包裝或產(chǎn)品上��。UDI-DI 必須登記在醫(yī)療器械數(shù)據(jù)庫中�����。

二��、新醫(yī)療器械CE認證法規(guī)(MDR)有關UDI的時間表:
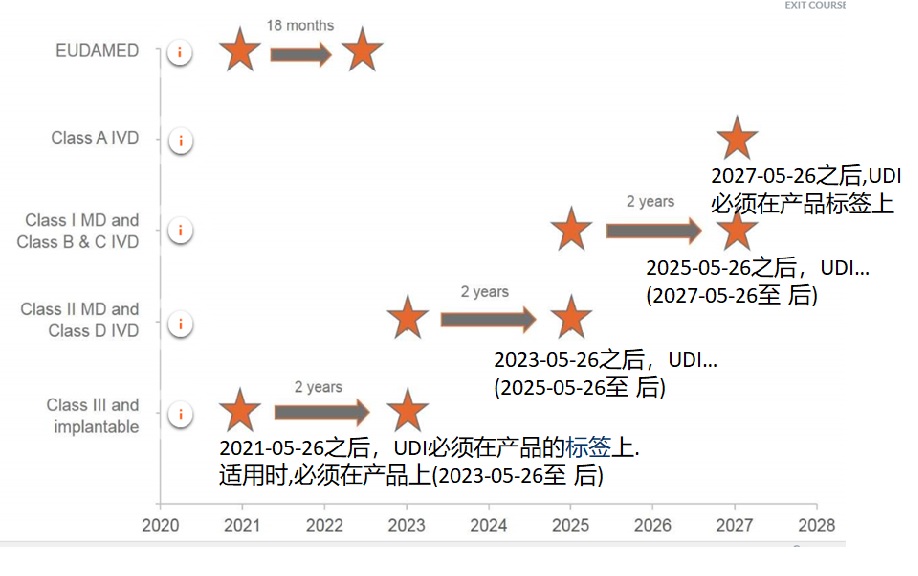
特別提醒的是���,關注醫(yī)療器械CE認證法規(guī)要求��,企業(yè)應該提前做好有關UDI的準備工作���。