醫(yī)用縫合針由GB/T 4240中規(guī)定的30Cr13��、40Cr13�����、12Cr18Ni9���、06Cr19Ni10牌號不銹鋼材料制造,用于縫合內臟、軟組織��、皮膚等�����,無菌提供����,一次性使用����。醫(yī)用縫合針在我國屬于第二類醫(yī)療器械注冊產品���,一起來了解醫(yī)用縫合針注冊要求�。
醫(yī)用縫合針由GB/T 4240中規(guī)定的30Cr13����、40Cr13、12Cr18Ni9��、06Cr19Ni10牌號不銹鋼材料制造,用于縫合內臟�����、軟組織����、皮膚等,無菌提供�����,一次性使用。醫(yī)用縫合針在我國屬于第二類醫(yī)療器械注冊產品��,一起來了解醫(yī)用縫合針注冊要求��。
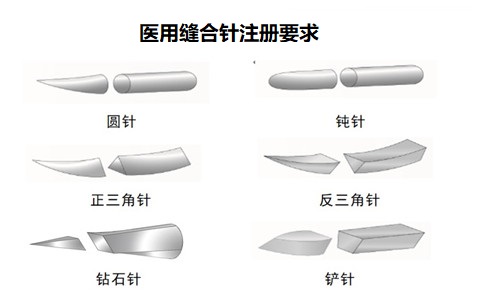
醫(yī)用縫合針注冊要求及審評要點:
1.醫(yī)用縫合針注冊單元的劃分
縫合針由針尖��、針體�����、針尾組成(見圖1)�,該產品一般一次性使用。根據《醫(yī)療器械分類目錄》��,申報產品分類編碼為02-07-01�。醫(yī)用縫合針注冊單元應以產品的技術原理�����、結構組成��、性能指標和適用范圍為劃分依據�。
如:不同牌號不銹鋼材料制作的縫合針可劃至同一注冊單元。通過鋒利的針尖結構進行穿刺�����、切割,經過針體的平滑過渡����,引導縫合線進行縫合。
2.產品技術要求
縫合針的基本技術性能指標主要參照YY/T 0043《醫(yī)用縫合針》��。在此基礎上�,申請人應根據產品的特點制定保證產品安全有效、質量可控的技術要求��,不適用部分應在研究資料中說明理由�。產品技術指標及試驗方法均應經過驗證。常見的技術指標包括但不限于以下內容:
2.1外觀
2.1.1針體
2.1.2三角刃口
2.1.3表面粗糙度
2.1.4彈機孔嵌線(如適用)
2.2物理性能
2.2.1硬度
2.2.2彈性
2.2.3韌性
2.2.4針尖強度(弦長L≥12mm的縫合針適用)
2.3使用性能
2.3.1刺穿力
2.3.2切割力
2.4初始污染菌(如適用)
2.5耐腐蝕性能
2.6滅菌(如適用)
2.7環(huán)氧乙烷殘留(如適用)
3.生物相容性評價研究
應參照GB/T 16886.1《醫(yī)療器械生物學評價 第1部分:風險管理過程中的評價與試驗》對成品(主要考慮與患者和使用者直接或間接接觸的材料)的生物相容性進行評價����。生物相容性評價研究資料應當包括:生物相容性評價的依據和方法,產品所用材料的描述及與人體接觸的性質����,實施或豁免生物學試驗的理由和論證,對于現有數據或試驗結果的評價��。
生物學評價過程中應當注重運用已有信息(包括材料�����、文獻資料、體外和體內試驗數據��、臨床經驗)�,當生物學評價確定需要進行生物學試驗時,應至少符合YY/T 0043以下要求:細胞毒性試驗反應不大于1級�;遲發(fā)型超敏反應應不大于1級;皮內反應計分應不大于1���。
4.滅菌工藝研究
4.1生產企業(yè)滅菌:應明確滅菌工藝(方法和參數)和無菌保證水平(SAL)���,并提供滅菌確認報告。器械的滅菌應通過GB 18279.1���、GB/T 18279.2或GB 18280.1、GB 18280.2�、GB/T 18280.3確認并進行常規(guī)控制,無菌保證水平(SAL)應保證達到1×10-6�。
4.2終端用戶滅菌:應當明確推薦的滅菌工藝(方法和參數)及所推薦的滅菌方法確定的依據。終端用戶滅菌的縫合針無菌保證水平(SAL)也應達到1×10-6��。
4.3殘留毒性:若滅菌使用的方法容易出現殘留����,如采用環(huán)氧乙烷滅菌���,應當明確殘留物信息及采取的處理方法,并提供研究資料�,企業(yè)需提供保證產品出廠時環(huán)氧乙烷殘留量不得大于10μg/g的處理方法。
4.4微生物控制:通過控制生產環(huán)境和生產過程保證初始污染菌水平��。若縫合針非滅菌提供���,其初始污染菌應小于等于100 CFU/件�;且應當提供證明包裝能減少產品受到微生物污染的風險�����,且適用于生產企業(yè)規(guī)定滅菌方法的研究資料���。
4.5滅菌過程的選擇應至少考慮以下因素:產品與滅菌過程間的適應性���;包裝材料與滅菌過程的適應性、滅菌對產品安全有效性的影響等���。
5.產品貨架有效期和包裝研究
5.1貨架有效期包括產品有效期和包裝有效期�。產品有效期驗證可采用實時老化或加速老化的研究。加速老化試驗研究的具體要求可參考YY/T 0681.1����,應遵循極限試驗等原則。在進行加速老化試驗研究時應注意:產品選擇的環(huán)境條件的老化機制應與宣稱的運輸儲存真實條件下發(fā)生產品老化的機制相匹配一致�����。
對于包裝的有效期驗證���,建議申請人提交在選擇恰當的材料和包裝結構合格后的最終成品包裝的初始完整性和維持完整性的檢測結果�。
5.2包裝及包裝完整性:在宣稱的有效期內以及運輸儲存條件下����,保持包裝完整性的依據。包裝材料的選擇應至少考慮以下因素:包裝材料的物理化學性能����;包裝材料的毒理學特性;包裝材料與產品的適應性��;包裝材料與成型和密封過程的適應性����;包裝材料與滅菌過程的適應性;包裝材料所能提供的物理����、化學和微生物屏障保護;包裝材料與使用者使用時的要求(如無菌開啟)的適應性��;包裝材料與標簽系統的適應性�����;包裝材料與正常貯存運輸途徑和過程的適合性����。可參考GB/T 19633��、YY/T 0681系列標準等����。