浙江省醫(yī)療器械注冊質(zhì)量管理體系核查時極具挑戰(zhàn)性事項�����,許多醫(yī)療器械行業(yè)從業(yè)人員說���,浙江省注冊體考可能是全國最嚴格的之一��,審查的專業(yè)而且細致���,因此����,要求企業(yè)不只是要有完備的文件和記錄���,不止是良好的硬件設施����,更看重人員的能力和素養(yǎng)���。本文為大家說說浙江省醫(yī)療器械注冊質(zhì)量管理體系核查要點之采購有什么要求�?一起看正文�����。
浙江省醫(yī)療器械注冊質(zhì)量管理體系核查時極具挑戰(zhàn)性事項�,許多醫(yī)療器械行業(yè)從業(yè)人員說,浙江省注冊體考可能是全國最嚴格的之一��,審查的專業(yè)而且細致���,因此�,要求企業(yè)不只是要有完備的文件和記錄��,不止是良好的硬件設施,更看重人員的能力和素養(yǎng)����。本文為大家說說浙江省醫(yī)療器械注冊質(zhì)量管理體系核查要點之采購有什么要求?一起看正文���。
浙江省醫(yī)療器械注冊質(zhì)量管理體系核查要點之采購有什么要求��?
一���、從醫(yī)療器械注冊質(zhì)量管理體系核查法規(guī)角度:
《醫(yī)療器械注冊質(zhì)量管理體系核查指南(2022年第50號)》規(guī)定:
“4.6采購
4.6.1(采購制度) 申請人應當建立采購控制程序,確保采購物品符合規(guī)定要求����。
4.6.2(原材料來源) 注冊檢驗產(chǎn)品及臨床試驗產(chǎn)品所需的原材料��,包括與產(chǎn)品直接接觸的包材����、軟件等應當具有合法來源證明,如供貨協(xié)議�����、訂單、發(fā)票����、入庫單、送貨單�����、批準證明性文件復印件等���。
4.6.3(主要物料采購) 主要原材料購入時間或者供貨時間應當與產(chǎn)品生產(chǎn)時間相對應���,購入量應當滿足產(chǎn)品生產(chǎn)需求,且應當有檢驗報告或者合格證明���。
4.6.4(采購記錄) 主要原材料的采購記錄應當符合產(chǎn)品設計需求和采購協(xié)議的規(guī)定���,記錄應真實、準確�、完整和可追溯。
4.6.5(體外診斷試劑采購記錄) 體外診斷試劑原材料的采購應當有采購合同或者采購記錄��。質(zhì)控品、校準品�、企業(yè)參考品的采購應滿足追溯要求,如涉及人體來源的樣本�,應當有相應原料的檢驗方法、檢驗過程�、檢驗數(shù)據(jù)、檢驗記錄���,以及表明生物安全性的證明材料等����。
4.6.6(體外診斷試劑關鍵物料要求) 體外診斷試劑設計定型后����,關鍵原材料本身如抗原(來源、氨基酸序列�����、構(gòu)象等)���、抗體(來源、細胞株等)�、引物探針序列等不應發(fā)生變化。”
二�����、從采購實務角度
醫(yī)療器械注冊質(zhì)量管理體系核查對于采購的核查重點包括三個模塊:
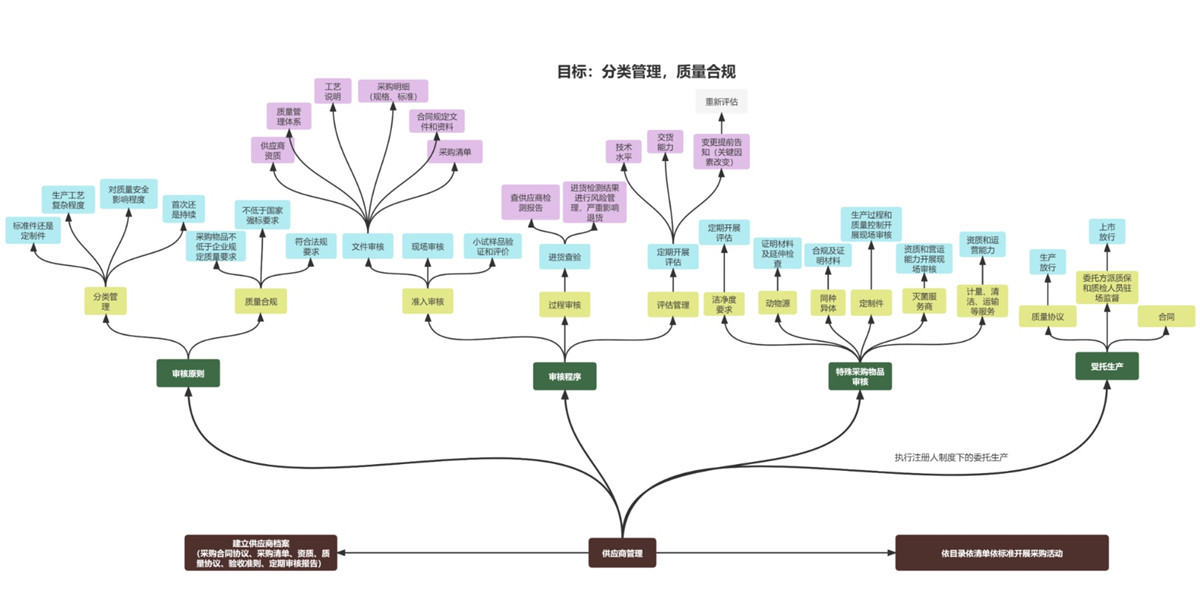
1.供應商管理:包括供應商的選擇���、評價和再評價�,及供應商的日常管理���;
2.采購執(zhí)行:核心是清晰表達采購要求并落實到位���;
3.采購物品的驗證:多數(shù)企業(yè)可能會與IQC來料檢驗一并處理。
浙江省醫(yī)療器械注冊質(zhì)量管理體系咨詢服務需求�����,歡迎您隨時方便與杭州證標客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡�,聯(lián)系人:葉工,電話:18058734169���,微信同��。