為幫助醫(yī)療器械注冊申請人更好地理解法規(guī)、規(guī)章��、指導(dǎo)原則等配套文件的要求��,上海器審中心統(tǒng)計了2022年度上海市第二類醫(yī)療器械注冊技術(shù)審評發(fā)補中的常見問題(無源醫(yī)療器械)��,并進行了歸類與剖析�����,以幫助注冊申請人提高注冊申報資料的科學(xué)性與合規(guī)性����,提高注冊申報的質(zhì)量和效率���。
為幫助醫(yī)療器械注冊申請人更好地理解法規(guī)�、規(guī)章����、指導(dǎo)原則等配套文件的要求,上海器審中心統(tǒng)計了2022年度上海市第二類醫(yī)療器械注冊技術(shù)審評發(fā)補中的常見問題(無源醫(yī)療器械)���,并進行了歸類與剖析��,以幫助注冊申請人提高注冊申報資料的科學(xué)性與合規(guī)性����,提高注冊申報的質(zhì)量和效率。
一����、2022年上海市第二類無源醫(yī)療器械注冊常見問題發(fā)補統(tǒng)計
2022年度,上海市器審中心共受理無源產(chǎn)品注冊申報共249件���。其中首次注冊發(fā)補率為100%����,變更注冊發(fā)補率為43.47%���,延續(xù)注冊發(fā)補率為33.7%���。
按照《關(guān)于公布醫(yī)療器械注冊申報資料要求和批準(zhǔn)證明文件格式的公告》(2021年第121號)的申報資料架構(gòu),小編將發(fā)補內(nèi)容進行了歸類和整理�。首次發(fā)布內(nèi)容的發(fā)補率見下表。
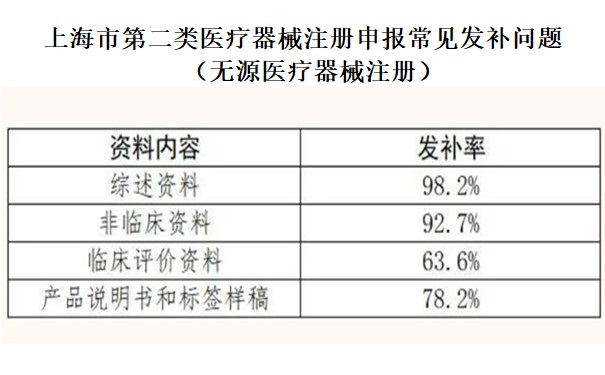
二�、2022年上海第二類醫(yī)療器械注冊常見發(fā)補問題分析(無源器械)
(一)綜述資料常見發(fā)補問題
1.醫(yī)療器械注冊單元
根據(jù)《醫(yī)療器械注冊單元劃分指導(dǎo)原則》的規(guī)定,產(chǎn)品的技術(shù)原理��、結(jié)構(gòu)組成、性能指標(biāo)���、適用范圍不同時�,原則上劃分為不同注冊單元�����。例如�,“液體敷料”存在西林瓶和預(yù)灌裝注射器兩種包裝形式,產(chǎn)品在結(jié)構(gòu)組成�、使用方法存在較大差異,建議作為不同的注冊單元進行注冊申報���。
2.產(chǎn)品名稱
產(chǎn)品名稱不符合《醫(yī)療器械通用名稱命名規(guī)則》和《醫(yī)療器械通用名稱命名指導(dǎo)原則》。例如����,“血栓抽吸連接管”應(yīng)修改為“一次性使用吸引連接管”。
3.產(chǎn)品作用機理
產(chǎn)品的作用原理描述含糊不清��,未提供詳細的作用機理說明或是各部件在產(chǎn)品中的功能�、各組件連接方式。例如�����,“導(dǎo)引鞘組”的各組件如何配合以實現(xiàn)產(chǎn)品的預(yù)期用途,建議給出產(chǎn)品原理圖和清晰示意圖��。
4.適用范圍
產(chǎn)品的適用范圍不規(guī)范���,未能根據(jù)分類目錄�����、分類界定文件�、免臨床評價目錄�����、已上市同類產(chǎn)品和產(chǎn)品臨床使用情況����,規(guī)范產(chǎn)品適用范圍。例如��,“負壓吸引連接管”與負壓吸引泵配合使用���,根據(jù)臨床實際使用在適用范圍中明確配套使用的負壓源情況�,給出產(chǎn)品能夠承受的最大負壓值。
5.結(jié)構(gòu)組成
產(chǎn)品的結(jié)構(gòu)組成不明確�,未能提供清晰示意圖。建議明確產(chǎn)品的具體結(jié)構(gòu)����,提交產(chǎn)品示意圖,標(biāo)注主要尺寸和組件名稱以及產(chǎn)品各組成部分的清晰圖片���。
6.型號規(guī)格
產(chǎn)品型號規(guī)格的設(shè)定依據(jù)不足����、不同規(guī)格之間的劃分不明確���,不同型號規(guī)格之間的差異描述不清楚��。例如�����,“潤滑劑”規(guī)格從5mL到1000mL,需要補充提交臨床應(yīng)用依據(jù)����,建議采用對比產(chǎn)品表對不同規(guī)格型號的結(jié)構(gòu)組成��、功能����、性能指標(biāo)加以描述��。
7.原材料
缺少產(chǎn)品原材料符合相關(guān)標(biāo)準(zhǔn)的支持性資料���。建議提供每個組件的原材料詳細信息��,包括原材料的等級規(guī)格�、質(zhì)量標(biāo)準(zhǔn)��、供應(yīng)商和入廠檢驗要求����;若生產(chǎn)過程中含有溶劑、粘結(jié)劑��、添加劑等��,應(yīng)進一步明確����。原材料如為液體�����,建議提供配比依據(jù)����,不同配方可能影響產(chǎn)品的基本性能�����。
(二)非臨床資料常見發(fā)補問題
1.產(chǎn)品技術(shù)要求
型號規(guī)格常見問題主要是:未明確型號規(guī)格劃分依據(jù)���。性能指標(biāo)發(fā)補問題有:①產(chǎn)品技術(shù)要求中的產(chǎn)品性能指標(biāo)低于適用的國家標(biāo)準(zhǔn)/行業(yè)標(biāo)準(zhǔn)��;②未采用最新發(fā)布的國家標(biāo)準(zhǔn)�、行業(yè)標(biāo)準(zhǔn)���;③與國行標(biāo)不一致或有缺漏適用項����;④檢驗方法與國家/行業(yè)標(biāo)準(zhǔn)不一致且未提交充分驗證依據(jù)�����。
2.檢驗報告
檢驗報告的典型性覆蓋問題較為常見��,如送檢樣品未能覆蓋全部的型號規(guī)格�����,建議除選擇典型型號進行全性能檢驗外���,還應(yīng)選擇其他型號進行差異性能檢驗��。
3.性能研究
①申請人往往對于產(chǎn)品技術(shù)要求中的性能指標(biāo)的研究�,僅提供了部分化學(xué)和物理性能編制研究資料���。例如��,企業(yè)提供了性能指標(biāo)的確定依據(jù)���,但未提供性能驗證方案和報告;②申請人未能提供對于產(chǎn)品安全性��、有效性存在一定影響���,但未納入產(chǎn)品技術(shù)要求的性能指標(biāo)中的其他性能研究資料���,例如:“一次性使用導(dǎo)引鞘”除產(chǎn)品技術(shù)要求中的性能指標(biāo)外���,還應(yīng)補充提交模擬使用相關(guān)的研究資料,如推送性能���、扭轉(zhuǎn)性能�����、回撤性能���、抗彎折性能、抗扭結(jié)性能等����;
4.生物相容性研究
①產(chǎn)品的生物相容性研究評價依據(jù)、接觸時間和與人體接觸的性質(zhì)等不明確�����,如僅提供原材料生物學(xué)試驗報告�,并非成品的生物學(xué)試驗報告���;②試驗樣品不具有代表性,如鼻塞導(dǎo)管僅選用成人型為代表型號����,該型號未覆蓋嬰兒型號的膠體貼片(直接接觸嬰兒皮膚)�。
5.滅菌研究
①提交的滅菌研究資料不完整,如:企業(yè)未能根據(jù)GB 18279系列標(biāo)準(zhǔn)提交滅菌確認方案和報告�、環(huán)氧乙烷的解析驗證方案及報告、相關(guān)過程記錄附件���;②所選滅菌產(chǎn)品不能代表注冊單元內(nèi)的所有規(guī)格型號�;③企業(yè)未能詳細描述過程挑戰(zhàn)裝置(IPCD和EPCD)的制備方法�����、明確BI的放置位置及最難滅菌位置的確定依據(jù)����;④關(guān)于滅菌產(chǎn)品的追加,應(yīng)根據(jù)GB 18279系列標(biāo)準(zhǔn)和YY/T 1268-2015《環(huán)氧乙烷滅菌的產(chǎn)品追加和過程等效》評估滅菌確認的產(chǎn)品是否能列入同一滅菌處理組�,并提供論證性資料,必要時應(yīng)對滅菌組內(nèi)的所有產(chǎn)品及其內(nèi)部挑戰(zhàn)裝置進行短周期抗性對比試驗以確認最難滅菌的產(chǎn)品����;不同滅菌柜也應(yīng)提交等效性驗證資料�;⑤產(chǎn)品經(jīng)全周期滅菌后應(yīng)對產(chǎn)品性能和包裝性能進行檢測��。如:企業(yè)未檢測滅菌后產(chǎn)品和包裝的全性能指標(biāo)��。
6.有效期和包裝研究
①應(yīng)依據(jù)《無菌醫(yī)療器械包裝試驗方法第1部分:加速老化試驗指南》(YY/T 0681.1)對產(chǎn)品(包括包裝)采用加速老化試驗和實時老化試驗的方式驗證其有效期���;②老化驗證報告應(yīng)包括但不限于���,加速老化起止時間、加速老化設(shè)備����、老化產(chǎn)品批號,并明確產(chǎn)品零時刻的檢驗報告和終時刻的檢驗報告�;③進行有效期驗證的產(chǎn)品應(yīng)能代表注冊單元內(nèi)的所有型號規(guī)格;④產(chǎn)品有效期驗證的檢測性能應(yīng)包含產(chǎn)品技術(shù)要求中的所有性能和包裝性能����,明確性能指標(biāo)和檢測方法,提交測試記錄���,并對加速老化過程中產(chǎn)品性能的變化進行分析���。⑤產(chǎn)品包裝驗證可依據(jù)有關(guān)標(biāo)準(zhǔn)進行(如GB/T 19633�����、YY/T 0681.1等)��,提交產(chǎn)品的包裝驗證報告。直接接觸產(chǎn)品的包裝材料的選擇應(yīng)至少考慮以下因素:包裝材料的物理化學(xué)性能���;包裝材料的毒理學(xué)特性�����、包裝材料與產(chǎn)品的適應(yīng)性�、包裝材料與成型和密封過程的適應(yīng)性�、包裝材料與標(biāo)簽系統(tǒng)的適應(yīng)性、包裝材料與貯存運輸過程的適應(yīng)性����。
(三)臨床評價資料常見發(fā)補問題
1.免臨床評價目錄
根據(jù)《免于臨床評價醫(yī)療器械目錄》內(nèi)容,注冊申請人應(yīng)提交申報產(chǎn)品與目錄產(chǎn)品的對比資料���,包括結(jié)構(gòu)組成�����、材質(zhì)���、適用范圍等信息��。
2.通過同品種臨床評價路徑進行臨床評價
對于與境內(nèi)已上市產(chǎn)品的對比項目中�,應(yīng)對其結(jié)構(gòu)差異�、型號規(guī)格、預(yù)期用途等進行詳細的分析評價�����,論證存在的差異是否會產(chǎn)生不同的安全有效性問題�,并提供科學(xué)依據(jù)和支持性資料。同時�,建議注冊申報人的比對資料詳細完整,不要使用“無明顯差異”“基本等同”等模糊描述��,對差異部分應(yīng)進行詳細論述��。
(四)產(chǎn)品說明書和標(biāo)簽樣稿常見發(fā)補問題
醫(yī)療器械產(chǎn)品說明書可參考以下具體文件《醫(yī)療器械說明書和標(biāo)簽管理規(guī)定》���、標(biāo)準(zhǔn)(強標(biāo)�、專標(biāo))及注冊技術(shù)審查指導(dǎo)原則對說明書的要求。常見發(fā)補問題如下:說明書中性能指標(biāo)與產(chǎn)品技術(shù)要求不一致�����;說明書中描述內(nèi)容��、適用范圍與綜述資料�����、研究資料不一致�;未涵蓋《醫(yī)療器械說明書和標(biāo)簽管理規(guī)定》中要求的內(nèi)容或描述不清晰�。
三、上海市2022年第二類醫(yī)療器械變更注冊常見發(fā)補問題分析(無源器械)
醫(yī)療器械變更注冊最常見發(fā)補問題是對變更內(nèi)容的驗證和確認不夠充分��,或表述不規(guī)范����。大部分問題與前文首次注冊常見問題相同,不再贅述�����。變更注冊特有的發(fā)補內(nèi)容如下:
(一)綜述資料常見發(fā)補問題
企業(yè)應(yīng)根據(jù)產(chǎn)品具體變更情況提供相應(yīng)的說明及對比表:型號規(guī)格變化����、產(chǎn)品名稱變化��、產(chǎn)品技術(shù)要求變化�、結(jié)構(gòu)及組成變化�����、產(chǎn)品適用范圍變化等�。特別注意如果新增型號規(guī)格與原有型號規(guī)格在結(jié)構(gòu)組成、性能指標(biāo)����、適用范圍等方面有顯著差異,不能作為同一注冊單元進行變更注冊��。
(二)研究資料常見發(fā)補問題
涉及新增型號規(guī)格��,需提交臨床設(shè)計的依據(jù)���,及相應(yīng)的性能研究����、滅菌研究、有效期研究�、臨床評價等方面的資料;涉及部件材料發(fā)生變化�����,需提交成品性能研究報告����、有效期驗證方案和報告,必要時提供生物學(xué)評價報告��;涉及變更滅菌方式�����,應(yīng)提供生物相容性研究資料�,以評估滅菌方式的改變是否會影響產(chǎn)品的生物相容性�����。
四��、上海市2022年第二類醫(yī)療器械器械延續(xù)注冊常見發(fā)補問題分析(無源器械)
延續(xù)注冊發(fā)補最主要問題是執(zhí)行的強制性標(biāo)準(zhǔn)����、《中華人民共和國藥典》版本已修訂���,但申請人未在產(chǎn)品技術(shù)要求中補充新要求并提供證明產(chǎn)品符合新要求的檢驗報告。該情況下�����,會在形式審查階段發(fā)出補正意見��。申請人應(yīng)持續(xù)關(guān)注新的強制性標(biāo)準(zhǔn)發(fā)布情況��,確保相關(guān)條款符合國家標(biāo)準(zhǔn)要求后再行延續(xù)注冊申報����。
五、總結(jié)與討論
本文對2022年上海市第二類體無源器械注冊申報常見發(fā)補問題進行了系統(tǒng)的梳理和分析��。無源產(chǎn)品種類繁多��,確認和驗證的過程較復(fù)雜�����,對申請人能力要求較高��。申請人應(yīng)深刻理解、準(zhǔn)確把握相關(guān)指導(dǎo)原則中的具體要求����,再實施驗證和確認,避免發(fā)補后重新進行驗證����,造成時間與資源的浪費。產(chǎn)品技術(shù)要求�、產(chǎn)品說明書、文字描述的規(guī)范性���、與注冊申報資料的一致性應(yīng)高度重視�����,仔細斟酌�����。由于新發(fā)布的《關(guān)于公布醫(yī)療器械注冊申報資料要求和批準(zhǔn)證明文件格式的公告(2021年第121號)》對綜述資料有了更具體的要求,申請人應(yīng)予以相應(yīng)關(guān)注�,避免出現(xiàn)資料完整性的問題。
標(biāo)簽:上海第二類醫(yī)療器械注冊�����、上海第二類醫(yī)療器械延續(xù)注冊、上海第二類醫(yī)療器械變更注冊